来たる2021年2月9日、弊社TFDA関連規制対応の責任者であるTravis Hsuによるセミナーを開催いたします。
<セミナー内容>
台湾の医療機器規制
TFDAについて
申請者に対する要求事項
QMS要求事項
製品登録
台湾の最新情報
<テュフズード様のセミナー案内>
https://www.tuvsud.com/ja-jp/services/training/ac/medical/open-schedule/taiwan
<セミナーパンフレット>
平素は格別のお引き立てを賜り、誠に有難うございます。
弊社の年末年始休業期間につきまして、下記の通りご案内申し上げます。
<休業期間>
2020年12月29日(火)から2021年1月3日(日)
新年は2021年1月4日(月)より平常通り営業いたします。
2021年も変わらぬお引き立ての程、何卒よろしくお願い申し上げます。
中国 NMPAは医療機器の監督管理強化の一環として2019年8月にUDI規則を公布しました。
2020年9月以降、下記のクラスIII(第三類)の医療機器から運用が開始となります。
|
一级产品类别 |
二级产品类别 |
管理类别 |
|
01骨结合植入物 |
02单/多部件可吸收骨固定器械 |
III |
|
03脊柱植入物 |
02脊柱椎体间固定/置换系统 |
III |
|
04关节置换植入物 |
01髋关节假体 |
III |
|
02膝关节假体 |
III |
|
|
03肩关节假体 |
III |
|
|
04肘关节假体 |
III |
|
|
05指关节假体 |
III |
|
|
06腕关节假体 |
III |
|
|
07踝关节假体 |
III |
|
|
08颞下颌关节假体 |
III |
当初、2020年10月から開始となっていましたが2021年1月へ延期となり、中国NMPAのUDIシステムへ登録する必要があります。
弊社では9月から医療機器メーカー様のUDIシステムへの登録をサポートさせていただいております。
一般的にはGS1標準に基づく表示になると考えますが、欧米・日本向けで検討されているUDIと発行機関をご連絡いただき、中国UDI対応のサポートをさせていただきます。
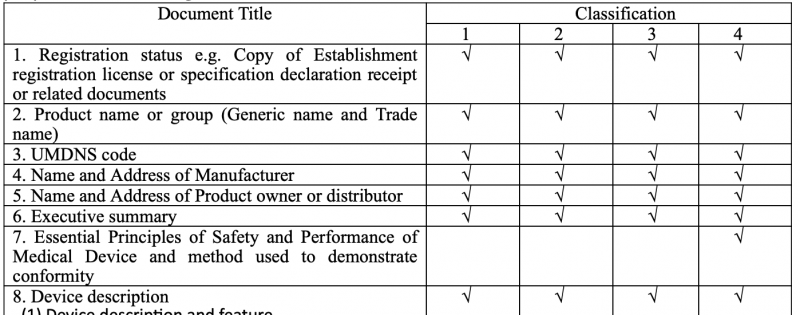
タイFDAは、登録済みの医療機器に対するCSDT検査実施の新たな通知を発表しました。
クラス1, 2, 3の医療機器について2021年6月21日から実施され、クラス4は2021年9月11日となります。
期日までにタイFDAからのCSDT検査に向けCSDT文書を完成させておく必要がございます。
※弊社が法定代理人のお客様につきましては、通知原文(参考英訳)をご案内いたします。
Notified/Licensedの医療機器輸入許可をお持ちの場合、既にCSDTで審査を受けられていると思いますが、General Medica Device (クラスIII)の医療機器メーカー様はご準備が必要です。
2021年1月1日以降、製造業者と医療機器はMHRAに登録される必要があります。
また、国外の製造業者は UK Responsible Person (UK REP)をイギリス国内に任命しなければなりません。
輸入者がそのままUK REPとなるのか、EUのように独立した第三者がUK REPになれるの議論されていますが、UK REPの選択・契約には時間もかかります。
弊社のパートナー企業をご紹介させていただくことも可能ですので、お気軽にお問い合わせください。
※現在、ビジネス継続の為に新規に任命・変更が必要なお客様を優先してご対応させていただいております。
来る2020年10月27日(火)、NPO海外医療機器技術協力会様主催のセミナーを開催いたします。
Web型式のセミナーとなります。
マレーシア、フィリピン、タイの最新医療機器規制のアップデートをご紹介いたします。
セミナー詳細は下記をご確認ください。
この度ASEAN医療機器薬事規制についてにオンラインセミナーを開催いたします。
本セミナーではASEAN各国における薬事承認から市販後調査までの基本を一貫してご紹介いたします。
参加をご希望の方はこちらこちらから登録をお願いいたします。
セミナー日時
2020年9月30日(水曜)12:45~14:15
当日のアジェンダ
- ASEANにおける医療機器の薬事承認
- シンガポール・マレーシア・フィリピン・ベトナム・インドネシア・タイにおける最新の医療機器規制
- 上記各国における現地法定代理人の役割
- 講演者:Qualtech Consulting Corporation グローバル薬事マネージャー Irene Lu
- 現地法定代理人・輸入業者・販売業者の責任Authorized Representative (AR), Importer, and Distributor’s Responsibilities in ASEAN
- ASEAN各国の比較:医療機器輸入に必要な条件・現地法定代理人が負う責任の違い
- GDP (実践流通規範) と現地法定代理人の選び方
- 講演者:Qualtech Consulting Corporation グローバル薬事チーム Eve Peng
- 市販後調査について
- ASEAN各国の規制当局の市販後調査のマネジメント
- 市販後調査の要件について
- 講演者: Qualtek Consulting Sdn. Bhd マレーシア支部薬事リーダー Yee Zi Hui
ご質問・ご不明点等ございましたらこちらまでお問い合わせください:このメールアドレスはスパムボットから保護されています。閲覧するにはJavaScriptを有効にする必要があります。
去る2020年9月1日、UK MHRAは医療機器・体外診断用医療機器のBREXIT後の規制について重要なガイダンスを発表しました。
本ガイダンスの重要な内容は以下となります。
1. Responsible Personをイギリス国内に製品通知の移行期間中に任命すること
製品通知の移行期間:
|
Class I Medical Device General IVD |
2022年1月1日 |
|
Class IIa, IIb List B IVD Self-test IVD |
2021年9月1日 |
|
Class IIb Class III Implant Active Implantable Medical Device List A IVD |
2021年5月1日 |
2. CEマーク製品は2023年6月30日まで認められる(Recognizeされる)・・・CEマークはDirective(指令)、Regulation(規則)を問わない
3. UK適合性評価マーク(UKCA)の導入、2023年7月1日以降はUKCAマークの強制化、及びUKが認めた機関による認証も強制
4. クラス I の医療機器は自己宣言が可能、2021年1月1日以降、UKCAマークの表示も可能。UKCAマークはUK MDR2002による。
5. MHRAは2021年から適合性評価機関を任命する。
去る2020年8月24日、特定のハイリスク・デバイスを取り扱う台湾の法定代理人・ライセンスホルダー 、販売代理店に対するGDP案を発表しました。
合計45の医療機器がリストされていますので、該当する医療機器を製造販売されている企業様はご注意ください。
https://gazette.nat.gov.tw/egFront/detail.do?metaid=117926&log=detailLog
預告「醫療器材管理法第二十四條應建立醫療器材優良運銷系統之醫療器材品項及其販賣業者」草案
MINISTRY OF HEALTH AND WELFARE Notice is hereby given, to commence a period of public comments for drafting "Medical Device Classification and Medical Device’s Dealers Shall Establish a Medical Device Good Distribution System Specified in Article 24 of Regulations for Governing the Management of Medical Device"
最近多くお問い合わせいただきます中国における製品回収、有害事象を検索できるリンクを下記までご案内いたします。
NMPAの医療機器回収通知
https://www.nmpa.gov.cn/xxgk/chpzhh/ylqxzhh/index.html
NMPAの医療機器有害事象
https://www.nmpa.gov.cn/xxgk/yjjsh/ylqxblshjtb/index.html
中国NMPAは現地試験所にて実施される電気安全規格について、国際規格のIEC60601-1:第3版に対応するGB9706.1:2020による試験を
2023年5月より実施いたします。
GB 9706.1-2020 (GB9706.1-2020)
Medical electrical equipment--Part 1: General requirements for basic safety and essential performance
現在、弊社スタッフも試験所のトレーニングに参加し、現地試験(立会試験)にて十分なサポートが出来るよう進めております。
各試験所の試験開始時期や新規申請・更新時の扱いなど、新たな詳細情報は弊社メールマガジン、最新ニュースにて更新いたします。
NMPAは8月末までフィードバックを受け付けています。
<リンク>
关于征求《2020年新增和修订的免于进行临床试验医疗器械目录(征求意见稿)》意见的通知
中国へ製品登録をしている医療機器ついて、2020年9月30日を期限として定期的リスクアセスメント報告書(中文)提出の要求事項が発表されました。
http://www.nmpa.gov.cn/WS04/CL2138/378540.html
主な内容は、製品の基本的な情報、国内外の上市条件、過去のリスク管理措置、有害事象報告情報、その他のリスク情報、製品リスク分析、要求されている期間の結論および付属書が含まれています。
日本の医療機器メーカー様は現地法定代理人を通じて期限までに報告書を提出する必要がございますので、ご注意ください。
香港のMDD(Medical Device DIvision)は、クラスII, III, IV機器の迅速承認スキームを継続します。
本スキームは本年12月31日まで継続します。
4つの条件:
1. There are no reported deaths or serious injury associated with the device (local and worldwide)
2. There are no active recalls, field safety corrective actions or adverse incidents (local and worldwide)
3. Two or more valid, independent regulatory agencies’ approval have been obtained for at least three years
4. There is at least one substantially equivalent device listed under the Medical Device Administrative Control System (MDACS)
<詳細リンク>
弊社では一部のお客様からのメール受信に遅延が発生した問題、また更なるセキュリティ対策の一環といたしまして、メールサーバーの更新を実施いたします。
つきましては、2020年6月11日(木) 午後5時より メールの送受信が制限されます。
翌日より通常通りとなりますので、予めご了承くださいませ。
ご迷惑をお掛けし誠に恐れ入りますが、何卒ご理解の程、よろしくお願い申し上げます。
弊社では一部のお客様からのメール受信に遅延が発生した問題、また更なるセキュリティ対策の一環といたしまして、メールサーバーの更新を実施いたします。
つきましては、2020年6月11日(木) 午後5時より メールの送受信が制限されます。
翌日より通常通りとなりますので、予めご了承くださいませ。
ご迷惑をお掛けし誠に恐れ入りますが、何卒ご理解の程、よろしくお願い申し上げます。
ドイツの規制当局はCOVID-19に関連する体外診断用テスト機器の登録機器をDIMDIで公開しています。
https://www.dimdi.de/dynamic/de/medizinprodukte/datenbankrecherche/corona-tests/
※本リストは毎日更新されています。
5月28日現在、277のコロナ関連の製品が届出されています。
アジアの医療機器メーカーの製品が数多く届出されていますので、欧州市場への事業展開の情報としてご活用ください。
CE対応につきましてもお気軽にお問い合わせください。
去る5月6日に発表されました 「リスク・アセスメント報告書提出に関する通知」について、第二類、三類の医療機器の製造業者様は、本年9月末までにNMPAへ登録済みの医療機器に関連する市販後の不具合事象に関するリスクアセスメントの報告書を提出する必要がございます。(第一類の医療機器は自己管理とする)
<Notice of Risk Assessment Report Submission>
http://www.cdr-adr.org.cn/tzgg_home/202005/t20200506_47347.html
これは、2018年8月31日に公布、2019年1月1日より施行された「医療機器不具合事故モニタリング、再評価管理方法」の第39条に関連しています。
《医疗器械不良事件监测和再评价管理办法》(国家市场监督管理总局令第1号)
弊社では、リスクアセスメント報告書(中文)の事前確認と翻訳の時間を考慮し、6月30日を目処に製造業様へ報告書の提出をお願いしております。
昨年はNMPAへの医療機器登録申請件数は2018年に比べ大幅に増加した年となりました。
(対2018年比)
1)合計申請数 9,104件(新規、更新、変更含む) (37.8%増)
2)輸入医療機器 申請件数
クラスII 3,053件(新規358、更新1,847、変更848) (43.7%増)
クラスIII 2,540件(新規280、更新1,457、変更803) (20.9%増)
3)輸入医療機器 登録件数
クラスII 2,754件(新規357、更新1,622、変更757)
クラスIII 2,540件(新規284、更新1,417、変更837)
詳細は弊社ホームページ(英語)にてご確認ください。